Articles
Solution IA au paradoxe de Levinthal
mars 2021
Le programme d’IA de DeepMind a résolu un problème biologique d’une complexité diabolique qui était resté non résolu pendant un demi-siècle, et a stupéfié les scientifiques en démontrant une capacité à prédire le repliement des protéines avec une précision incroyable.
« Alphafold 2 », un outil d’intelligence artificielle pour générer des modèles 3D de protéines basés sur des jeux de données génomiques, a été annoncé en novembre 2020 et salué comme l’une des technologies scientifiques les plus révolutionnaires de notre époque, permettant aux scientifiques de voir comment une protéine se repliera en se basant uniquement sur sa séquence d’acides aminés primaire sans avoir besoin de techniques de laboratoire laborieuses. Mais quels sont les problèmes liés à la PI générée par un outil si utile ?
Percée
DeepMind est une société d’IA fondée à Londres en 2010 pour se concentrer sur l’apprentissage automatique et les neurosciences systémiques avec une vision de « faire penser les ordinateurs comme les humains » et a été acquise par Google en 2014. DeepMind a connu un succès largement médiatisé en 2015 avec son programme AlphaGo, qui fut le premier programme informatique à battre un joueur de Go humain professionnel, et développe plus récemment un outil d’intelligence artificielle qui prédit le repliement des protéines à partir d’une séquence d’acides aminés primaire uniquement. La dernière version de l’outil, nommée « AlphaFold 2 », a récemment obtenu des résultats stupéfiants lors du défi annuel de prédiction de structure protéique, CASP [1].
Les résultats du défi sont annoncés chaque année lors de la conférence annuelle qui a lieu depuis 1994, et l’équipe qui fournit la prédiction structurelle la plus précise est proclamée gagnante. En 2020, AlphaFold 2 a surpassé toutes les autres équipes avec une marge considérable, atteignant un score de 92,4 GDT (sur 100) globalement sur toutes les cibles, ce qui signifie que ses prédictions ont une erreur moyenne (RMSD) de seulement 1,6 Angströms [2].
Pourquoi cela est-il significatif ?
Les scientifiques utilisent déjà l’outil pour résoudre des structures protéiques avec lesquelles ils ont eu des difficultés pendant des années, mais en quelques heures seulement. La structure des protéines est généralement étudiée en cristallisant la protéine et en la visualisant à l’aide de la cristallographie aux rayons X ou plus récemment de la microscopie cryo-électronique et de la RMN. Cependant, ce processus est lent, laborieux et coûteux, et certaines protéines peuvent être difficiles à cristalliser, comme celles intégrées dans les membranes. Cette difficulté est parfois appelée le paradoxe de Levinthal ; Levinthal a estimé 10
AlphaFold 2 accélère considérablement le processus de compréhension de la façon dont une protéine se replie et de son apparence dans l’espace 3D basé uniquement sur la séquence d’acides aminés primaire.
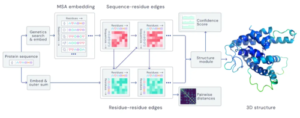
Figure 1 : la base du système AlphaFold 2 (crédit image : https://en.wikipedia.org/w/index.php?curid=65998083)
La visualisation de la structure protéique a des utilisations dans la compréhension de la façon dont les interactions cellulaires se produisent. En particulier, comment les protéines se lient à d’autres molécules et remplissent leurs fonctions, et quelles parties de la structure protéique sont essentielles à cela. En essence, on pense que la façon dont une protéine fonctionne est largement déterminée par sa forme 3D.
Avoir de telles connaissances facilement accessibles fera progresser de nombreux domaines de recherche en sciences de la vie et conduira probablement à de nombreuses nouvelles thérapies. Cela accélérera la découverte de médicaments dans laquelle les médicaments candidats sont souvent criblés pour leur liaison à une protéine particulière, généralement pour modifier sa fonction in vivo, et fournir un effet thérapeutique. Cela accélérera également le développement de nouvelles conceptions de protéines utiles, où, par exemple, un résidu particulier qui est essentiel à la fonction peut être modifié pour augmenter ou diminuer son activité. Cela aidera également à accélérer l’identification des différences structurelles résultant de variations génétiques causant des maladies, aidant à arriver plus rapidement à des traitements pour de telles maladies génétiques. Il est compréhensible que cette avancée soit saluée comme l’une des percées les plus significatives du siècle.
Problèmes potentiels de PI
Étant donné les avantages significatifs d’AlphaFold 2, de nombreuses inventions résulteront sans aucun doute de son utilisation. De nouveaux médicaments à petites molécules, de nouvelles protéines et leurs utilisations médicales ou industrielles n’en sont que quelques-unes. Cependant, de telles inventions sont-elles brevetables, et quels sont les problèmes potentiels avec la brevetabilité ? De plus, si une IA crée de la propriété intellectuelle telle qu’une invention, ou une partie d’une invention, est-elle un inventeur même si elle n’est pas une personne ? S’il n’y a pas d’inventeur humain, alors l’invention peut-elle être brevetée du tout ?
Brevetabilité
En laissant de côté la question de l’invention pour l’instant, il est indéniablement possible que de nombreuses inventions liées à l’IA soient protégées par un brevet en Europe. Pour être brevetable, il est nécessaire qu’une invention liée à l’IA fournisse un effet technique, qui peut être, par exemple, basé sur une application réelle d’un outil d’IA, la sortie d’un outil d’IA, une façon innovante de préparer des données d’entraînement pour l’entrée dans un système d’IA, ou même un arrangement matériel de traitement d’IA innovant
Cependant, l’utilisation d’AlphaFold 2, tout comme d’autres programmes de modélisation in silico, soulève peut-être des questions sur la façon dont l’activité inventive est évaluée. En particulier, étant donné qu’un outil existe maintenant pour résoudre la structure des protéines rapidement et facilement, il y a certainement moins de difficulté associée à l’analyse des protéines et à l’identification de solutions utiles directement à partir de telles structures. Il est donc possible que les offices de brevets considèrent les solutions résultant de la réalisation qu’une protéine donnée se lie à un certain partenaire tel qu’un récepteur ou un médicament comme plus évidentes, lorsque la structure montre clairement une région de liaison connue pour de tels partenaires, et lorsque le criblage pour la liaison pourrait potentiellement être fait entièrement in silico. En d’autres termes, lorsqu’un outil d’IA est facilement disponible pour prédire une structure protéique in silico, le seuil d’activité inventive devrait-il être relevé par rapport à l’activité inventive requise si l’algorithme de repliement de protéines d’IA n’avait pas été disponible ?
Les avancées dans les prédictions de repliement de protéines pourraient également donner lieu à une augmentation des revendications de portée « insuffisante » – des revendications qui couvrent des protéines nouvelles potentielles et/ou des utilisations potentielles de la protéine qui ont été identifiées à l’aide de l’outil d’IA, mais qui n’ont pas réellement été testées et démontrées comme fonctionnelles. Par exemple, cette situation pourrait survenir si les chercheurs devaient utiliser AlphaFold 2 pour identifier la structure 3D d’une nouvelle protéine, émettre des hypothèses sur ce à quoi elle pourrait se lier et inférer les utilisations potentielles résultantes, puis tenter de revendiquer ces utilisations sans tests supplémentaires. Alternativement, des revendications peuvent être déposées qui tentent de couvrir tout partenaire de liaison d’une structure protéique résolue donnée qui pourrait être utile. De telles revendications étaient répandues lorsque la technologie de clonage et de séquençage génétique est devenue largement répandue dans les années 1980, permettant aux scientifiques d’identifier des gènes qui n’avaient pas été identifiés auparavant. De nombreux demandeurs ont tenté de revendiquer ces séquences génétiques et leurs utilisations hypothétiques basées uniquement sur les informations de séquence [4]. Dans certains cas aux États-Unis, des demandes ont été déposées dans lesquelles des milliers d’étiquettes de séquence étaient couvertes qui n’avaient aucune fonction connue. Ce type de revendication est maintenant considéré comme manquant d’habilitation ou de support s’il n’y a pas de données appropriées démontrant une utilisation technique pour la séquence isolée. Nous pourrions bien voir une augmentation de tels dépôts spéculatifs une fois de plus, mais cette fois basés sur les protéines plutôt que sur les gènes.
Invention par IA
Il semblerait, au moins pour le moment, que l’outil AlphaFold 2 soit destiné à aider les efforts inventifs des scientifiques humains plutôt qu’à concevoir des inventions de manière autonome. En conséquence, il semble probable que les inventions dérivées à l’aide de l’outil AlphaFold 2 auraient encore des inventeurs humains. Cela dit, il est peut-être possible que les développements futurs du système AlphaFold puissent être plus autonomes, par exemple en déterminant la structure protéique et en la traitant pour trouver les partenaires de liaison ou les applications particulières sans l’expertise des scientifiques. Lorsque les humains testent simplement l’adéquation d’une liste restreinte de molécules suggérées produites par un tel outil d’IA pour leurs applications associées, identifier l’invention humaine pourrait potentiellement devenir plus difficile.
Dans une récision récente de la Haute Cour du Royaume-Uni [3], M. le Juge Smith a statué qu’une machine d’IA nommée « DABUS » ne pouvait pas être considérée comme un « inventeur » sous le UK Patents Act 1977 parce qu’elle n’est pas une personne physique et parce que, en tout état de cause, le droit d’obtenir une demande de brevet ne pouvait pas être transféré d’un inventeur IA à un demandeur de brevet parce qu’un inventeur IA manquerait de la « personnalité juridique » nécessaire pour posséder et transférer des droits de propriété. L’Office européen des brevets est arrivé à une décision similaire concernant les demandes de brevet européen correspondantes déposées nommant DABUS comme seul inventeur, bien que ces cas soient maintenant en appel. Ainsi, le système de brevets en Europe ne reconnaît généralement pas (du moins pas encore) les inventeurs IA.
Cependant, il y a encore des questions légitimes concernant qui devrait être légitimement nommé comme inventeur dans les cas où une entité IA fait « l’invention ». La décision de la Haute Cour du Royaume-Uni de M. le Juge Smith a positivement laissé ouverte la possibilité que le propriétaire d’une machine IA qui « invente » quelque chose puisse être nommé comme inventeur (plutôt que l’entité IA elle-même). Cela permettrait potentiellement aux inventions faites principalement par des machines IA, où le propriétaire de la machine IA a contribué de manière minimale ou pas du tout à la distinction inventive par rapport à l’état de la technique, d’être brevetées par leurs propriétaires au Royaume-Uni à l’avenir. Un développement supplémentaire de la jurisprudence dans ce domaine (à la fois au Royaume-Uni et en Europe) est anticipé au cours des années à venir, ce qui apportera espérons-le plus de certitude aux demandeurs de brevets.
Conclusion
AlphaFold 2 démontre les avancées scientifiques révolutionnaires qui sont réalisables avec l’IA, et nous nous attendons à ce que de tels outils d’IA ouvrent de nouveaux domaines de technologie à explorer pour les scientifiques et les ingénieurs. Même alors que les systèmes de brevets du monde entier s’adaptent à la hâte pour suivre le rythme des développements technologiques qui dépassent souvent le droit des brevets, de nombreuses inventions liées à l’IA sont brevetables et les demandes de brevet dans ce domaine ont explosé mondialement. Cependant, il reste certaines questions, et il sera intéressant de voir comment les scientifiques utiliseront l’IA pour rechercher et générer de nouvelles thérapies.
[1] https://en.wikipedia.org/wiki/AlphaFold
[2] https://deepmind.com/blog/article/alphafold-a-solution-to-a-50-year-old-grand-challenge-in-biology
[3] https://www.bailii.org/ew/cases/EWHC/Patents/2020/2412.html
[4] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2220018/
Cet article a été préparé par les Directeurs de Brevets Senior d’HGF Eleanor Purnell et Dr Andrew McGettrick.


























